
TRPA1は末梢神経では冷覚や炎症時の痛みを受容するイオンチャネルです。冷情報などを受容してこれらのチャネルを発現した末梢神経(C線維)に活動電位が発生すると、その情報は脊髄後角表層のニューロンに伝えられます。末梢神経(C線維)は後角表層のニューロンとシナプス結合し、グルタミン酸受容体を介した興奮性のシナプス伝達を行います。我々はTRPA1が末梢だけでなく脊髄のシナプス終末部にも発現し、TRPA1を活性化すると特定の形態をもつ表層のニューロンへの情報伝達が、高度で洗練された神経回路によって制御されることを発見しました。
歌君が学位の研究テーマとして主にこの研究を行い、論文が受理されました。
Uta D, Furue H*, Pickering A.E, Rashid M.H,Mizuguchi-Takase H, Katafuchi
T, Imoto K, Yoshimura M. TRPA1-expressing primary afferents synapse with
a morphologically identified subclass of substantia gelatinosa neurons
in the adult rat spinal cord. European Journal of Neuroscience, 31(11):
1960-1973, 2010
脊髄のTRPA1チャネルを活性化すると、C線維終末部からの微小なグルタミン酸放出を促進するが、一方で、末梢からC線維を介した痛みの伝達は完全にブロックする!脊髄には痛みの伝達を高度に制御する神経回路があることが分かりました。この回路を賦活化すると末梢から脊髄への痛みの伝達が有効に抑えられることが示唆されました。
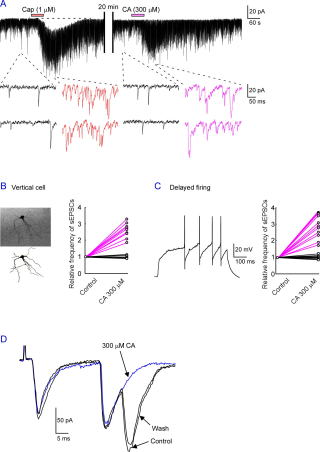
A. TRPV1作動薬であるカプサイシン(Cap; 1 mM)とシナモンオイル(CA; 300 mM)に対する自発性の興奮性シナプス後電流(spontaneous
excitatory postsynaptic currents; sEPSCs)の連発誘発応答を示した膠様質(substantia gelatinosa;
SG)細胞の代表例を示したものです。拡大した時間軸で示した下の記録は、コントロール時とそれぞれの作動薬存在下におけるsEPSCsを示しています。Capを投与するとsEPSCsの発生頻度が著明に増加し内向き電流も観察されます(左トレース)。さらに同一の細胞でCAを投与するとsEPSCsの発生頻度と振幅が著明に増加しましたが、Capのような内向き電流は見られませんでした(右トレース)。
B. 電気生理学的実験後にニューロビオチン染色されたvertical細胞の代表例とvertical細胞におけるsEPSCsに対するCAの作用を示した図です。写真は興奮性介在細胞と言われているvertical細胞です。写真の下の図は、カメラルシーダによって描写したものです。写真では分かりにくい樹状突起や軸索を示すことが出来ます。この細胞にCA(300
mM)を投与するとほとんどの細胞でsEPSCsの発生頻度の増加が見られました。
C. SG細胞の発火パターンの一例とその発火パターンにおけるsEPSCsに対するCAの作用を示した図です。脱分極性の電流パルス注入に応答してdelayed発火タイプを示した細胞例です。細胞形態と発火パターンを調べた過去の報告では、delayed発火タイプを示した細胞はvertical細胞であることが示されています。Delayed発火タイプを示した細胞にCA(300
mM)と投与するとほとんどの細胞でsEPSCsの発生頻度の増加が見られました。
D. 1つのAdelta線維誘起の単シナプス性EPSCと2つのC線維誘起の単シナプス性EPSCに対するCAの作用を示した代表例です。CA(300
mM)の投与によって、2番目のC線維誘起の単シナプス性EPSCが完全にそして選択的に抑制されました。


