量子化学計算を用いた酵素反応機構の解明
量子化学計算は汎用ソフトGaussianの開発以来、40年以上にわたって化学物質の構造、エネルギーおよび各種の物性値を求めるために用いられてきました。量子化学計算には高い精度でこれらの値を与える反面、多くの計算コストを必要とするという欠点があり、大きな分子を扱うことは長い間困難でありました。しかし近年、精度が高い量子化学計算を短時間で計算を行うことができる分子力学計算と組み合わせるマルチスケールモデルを用いた方法が開発され、酵素反応のように生体高分子の内部で起こる化学反応を計算することができるようになってきました。
現在私たちは、マルチスケールモデルを用いた量子化学計算によって、以下の生体反応の機構を明らかにすることを目標としています。
1. リボソームにおけるペプチド結合形成のメカニズムの解明
リボソームのX線結晶構造解析は2000頃に Yonath, Steitz, Ramakrishnan (2009年ノーベル化学賞受賞)らによって行われ、ペプチド結合形成反応の活性中心である Peptidyl Transferase Center (PTC) を構成する各原子の空間的な配置もすでに明らかにされています。
そこで私たちは、X線で明らかにされたPTCの構造に基づいて、リボソームの活性中心におけるペプチド結合形成のメカニズムをマルチスケールモデル法の一つである ONIOM法を用いて計算しています。これまでにすでに二段階機構の反応中間体や遷移状態における反応基質の最適化構造を明らかにしましたが、現在はさらに計算結果の信頼性を高めるべく、計算条件の検討を行っています。
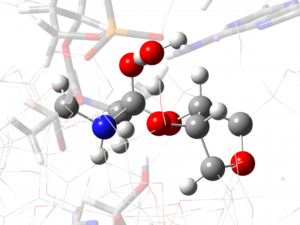
2. D-アミノ酸酸化酵素の反応機構の解明
D-アミノ酸酸化酵素は生体内にわずかしかないD-アミノ酸を選択的に酸化分解する酵素であるが、近年生体内におけるD-アミノ酸の生理的な役割が明らかにされるとともに、その重要性が再認識されてきています。
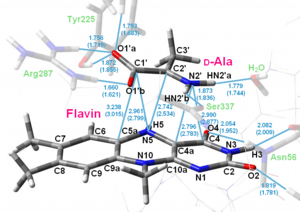
この酵素の反応では、酸化の際にD-アミノ酸の位の水素がヒドリドとしてフラビン補酵素に引き抜かれますが、そこで生じるイミノ酸と還元型フラビンアニオンとの間で安定な電荷移動(CT)錯体が生成するため、基質を加えると酵素が紫色に着色することが知られています。
現在、反応機構解明の手始めとして、ONIOM法によってこの電荷移動錯体の最適化構造を求め、電荷移動錯体における電子構造や電荷移動相互作用の詳細について検討を行っています。
有機金属触媒を用いる新規化学反応の開発
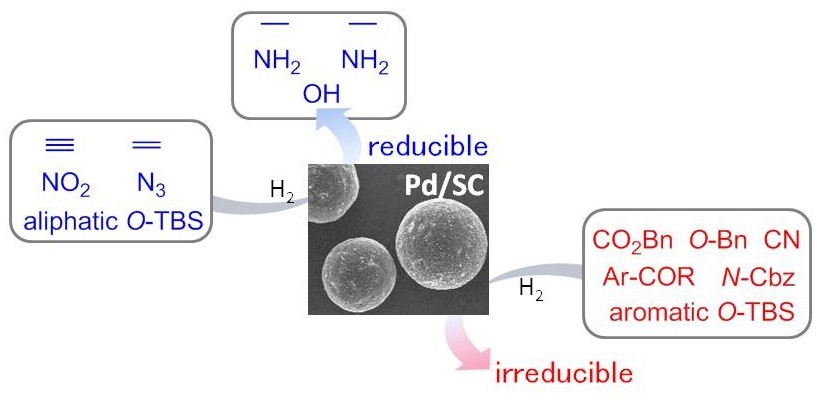
反応溶液に溶けずに作用する不均一系触媒は、均一系触媒と比較して触媒の安定性や最終生成物への金属の残留等の問題が少ない、再利用可能であるといった多くの利点を有しており、環境負荷低減型の触媒として注目されている。近年、高価な遷移金属触媒の再利用をさらに効率よく行うため、ポリマー等に担持させた触媒も開発されているが、反応活性の点で劣り、実用化は困難であるのが現状である。
現在、フィルム状のパラジウム触媒膜を利用した鈴木-宮浦反応や、球状に形成した活性炭にパラジウムを担持した触媒を利用した官能基選択的接触還元反応といった新しい反応の開発に取り組んでいる。(岐阜薬科大学薬品化学研究室佐治木研究室との共同研究)
 HOME
HOME RESEARCH
RESEARCH PUBLICATION
PUBLICATION UNDERGRADUATE
UNDERGRADUATE MEMBER
MEMBER GALLERY
GALLERY ACCESS
ACCESS
 兵庫医科大学
兵庫医科大学