STUDENTS 研究について 糖尿病・内分泌・代謝内科
-
概要
糖尿病グループと内分泌・代謝グループが連携して、基礎的・臨床的研究を活発に行っています。2019年4月から2022年3月の3年間は、兵庫医科大学横断プロジェクト「Hyogo Innovative Challenge」に中心的に関わりました。臨床研究としては、古典的な危険因子に加えて、睡眠などの社会的ストレスに関連した臨床因子も定量的に評価し、様々な糖代謝・内分泌疾患、心血管疾患、腎機能障害、肝機能障害、認知機能障害などとの関連を明らかにする2つのコホート研究を、精力的に推進しています。
さらに、先進糖尿病医療(持続血糖モニター、CSIIなど)の開発、尿酸・核酸代謝、副腎疾患などに関する研究を継続的に行っています。基礎研究では終末糖化産物受容体(RAGE)や、睡眠の質の意義に着目した研究を学内外の多くの研究グループと共同研究を実施しています。
専門領域の医師はもちろんですが、糖尿病療養指導士(看護師、栄養士、薬剤師など)の大学院博士課程の研究も積極的にサポートしています。 -
臨床研究
1.糖尿病患者における低血糖を含めた血糖変動と糖尿病合併症との関連についての多施設共同研究
(Hyogo Diabetes Hypoglycemia CognitionComplications study: HDHCC研究)糖尿病などの代謝異常患者に対して、生理学的バイオマーカーを網羅的に測定・追跡し、認知機能や合併症との関連を明らかにすることを目的としたHyogo Diabetes Hypoglycemia Cognition Complications study(HDHCC)多施設共同コホート研究を2018年から実施しています。2022年3月現在で483名が登録され、現在も新規登録と追跡を並行して実施しています。持続血糖モニター(CGM)を用いた血糖変動をはじめ、日中活動度及び睡眠状況の他覚的評価、腸内細菌叢とその代謝産物、夜間低血糖発症、糖尿病合併症進展、質問紙や画像検査による認知機能を総合的に評価しています。
これまでに、①糖尿病罹病期間と合併症の有無がCGMに基づく血糖管理目標の指標の悪化に関連していること、②低血糖リスクのある糖尿病薬の使用は特に高齢者における管理目標範囲を下回らせるリスクがあることを報告しました(kuroda N, et al. J Diabetes Investig. 2021, 12: 244-253)。
また、以前から実施している1型糖尿病コホートとの統合解析により、病型により通常臨床的に汎用されているHbA1c、グリクアルブミンなどの指標と血糖変動の関連を明らかにしました(Ohigashi M et al: J Diabetes Investig. 2021, 12:940-949)。
最近には、臨床的な血糖変動の意義に関する総説をまとめています(Kusunoki Y, et al: Intern Med 2022, 61:281-290)。
今後は特に認知機能との関連についての様々な知見が得られるものと期待しており、認知機能低下予防のターゲットが見出せるものと期待しています。学内の病原微生物学、及び学外の理化学研究所、筑波大学国際統合睡眠医科学研究機構との共同研究として実施しています。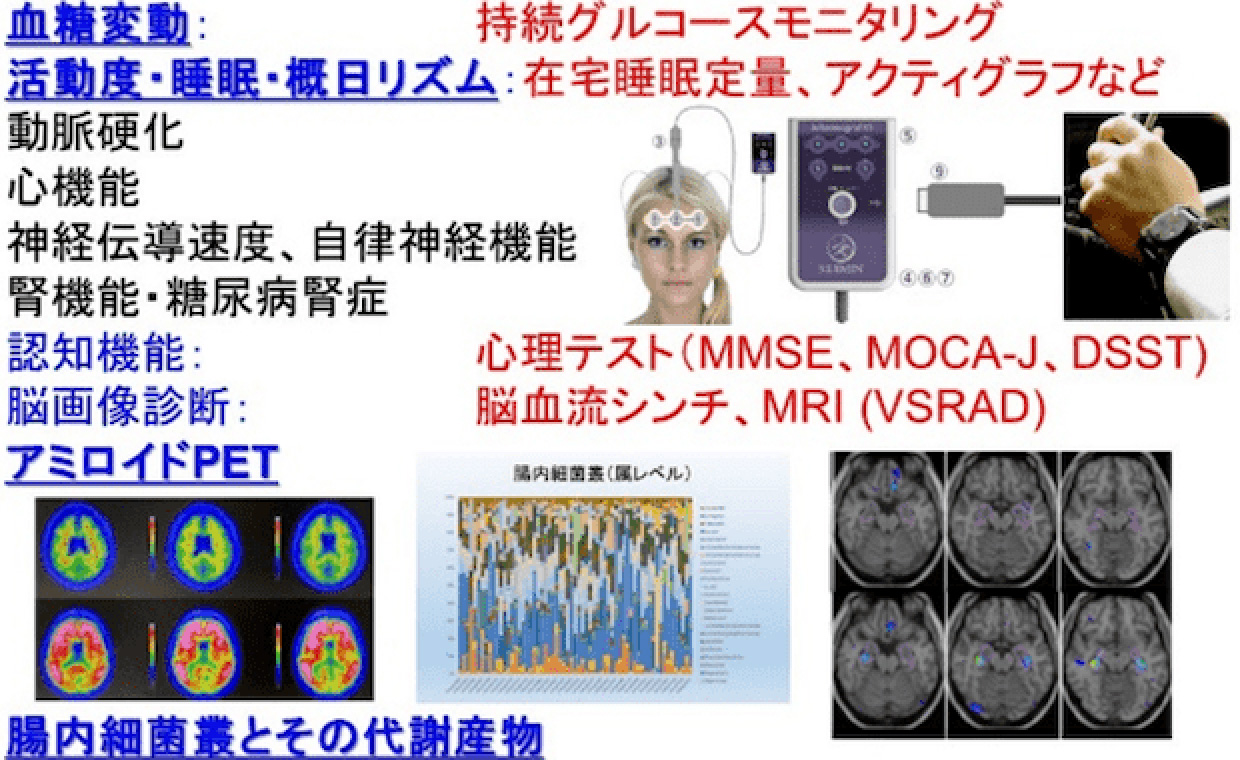
2.睡眠、疲労、自律神経機能などの生活関連因子が及ぼす生体ストレス応答研究
(Hyogo Sleep Cardio-Autonomic Atherosclerosis Study:HSCAA研究)日々の睡眠や疲労度、日中活動度、自律神経機能を客観的、網羅的に評価し、内分泌・代謝疾患の病態・予後を追跡し、睡眠や疲労、自律神経機能障害など生体ストレスの意義を明らかにすることを目的としたHyogo Sleep Cardio-Autonomic Atherosclerosis (HSCAA)コホート研究を2010年から実施しています。2022年度3月時点で約1,200人の患者が登録され、平均3.5年の追跡を受けています。これまでに、12編の論文、1編の総説を報告してきました。
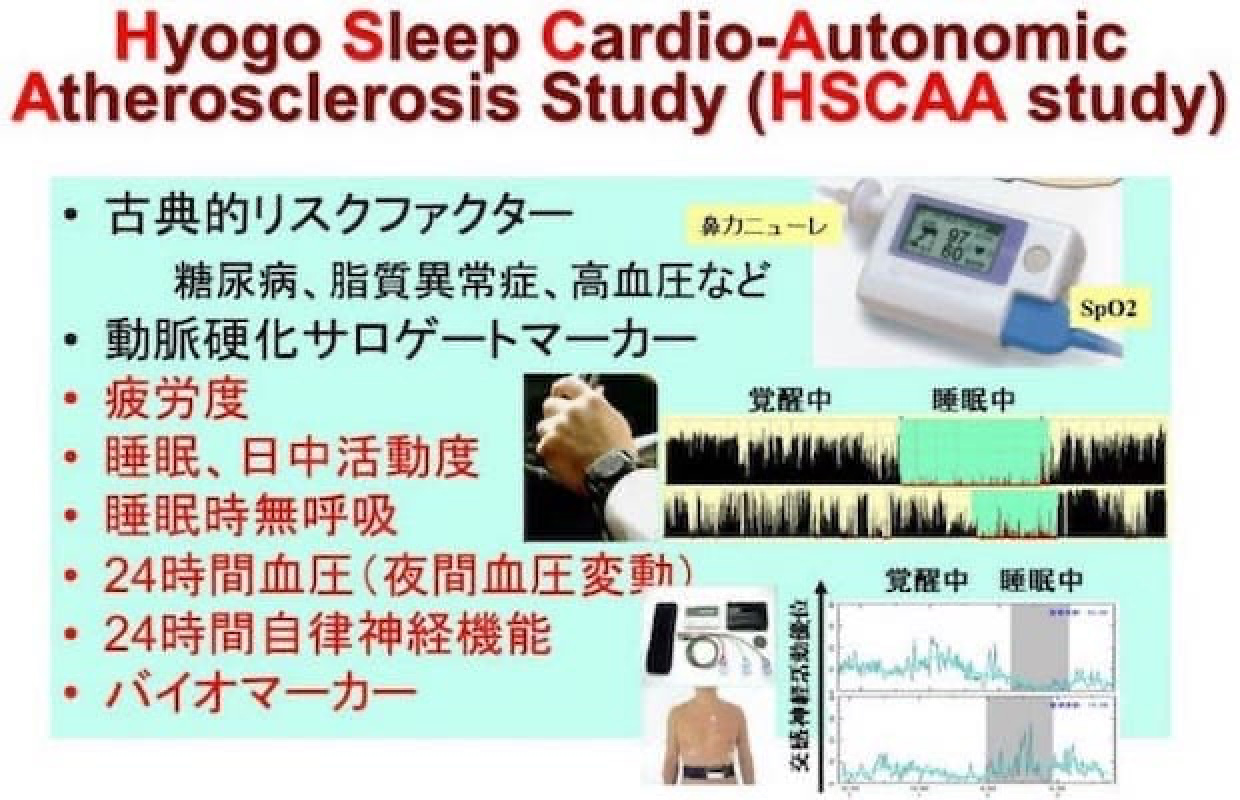
最近では、睡眠の「質」の低下がインスリン分泌能及び感受性低下と関連すること(Kakutani-Hatayama M, et al. Metabolism Open 2020, 6:100033)、自律神経機能と左室拡張能の指標との関連(Morimoto A, et al.Metabolism Open 2020, 5: 100025)、腎機能障害を有していない糖尿病患者での睡眠の「質」の低下及び自律神経機能障害の腎機能悪化のリスクについて相次いで報告しました(Kadoya M et al. Sci Rep2021, 11: 19048)。
今後も引き続きデータの集積を重ね、様々な代謝・内分泌疾患との関連、さらに心・腎・肝の様々な機能への影響についての新しい知見を発信する予定です。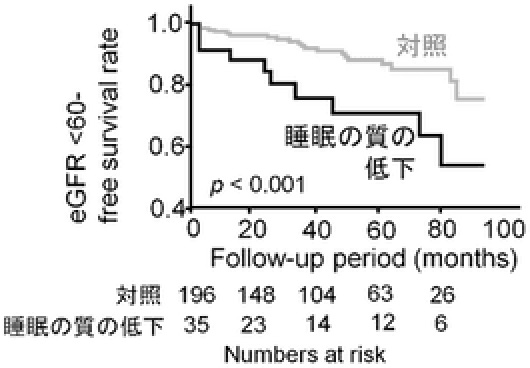
3.持続皮下インスリン注入(CSII)療法など先進的インスリン治療法の開発とその意義に関する研究
難波光義前主任教授が注力され、講座で脈々と継続されている研究テーマです。CSII(ContinuousSubcutaneous Insulin Infusion)およびSAP(Sensor Augmented Pump)療法の適正な使用方法や注入プログラムについて検証を行っています。
さらに、次世代のグルコースモニターやインスリンポンプの開発・検証も行っています。そのほか、新たなインスリンデバイスの臨床評価と個々の患者に最適なインスリン投与システムの構築をめざした研究を続けています。
4.核酸代謝の病態、特にXOR活性の代謝への影響に関する研究
山本徹也前内分泌・代謝科教授が精力的に進めてこられた、核酸代謝の病態に関する基礎的・臨床的研究を引き続き推進しています。
現在、当科では尿酸の合成と活性酸素種の生成を調節する酵素であるXanthine oxidoreductase(XOR)をターゲットとして、三和化学研究所との共同研究を実施しています。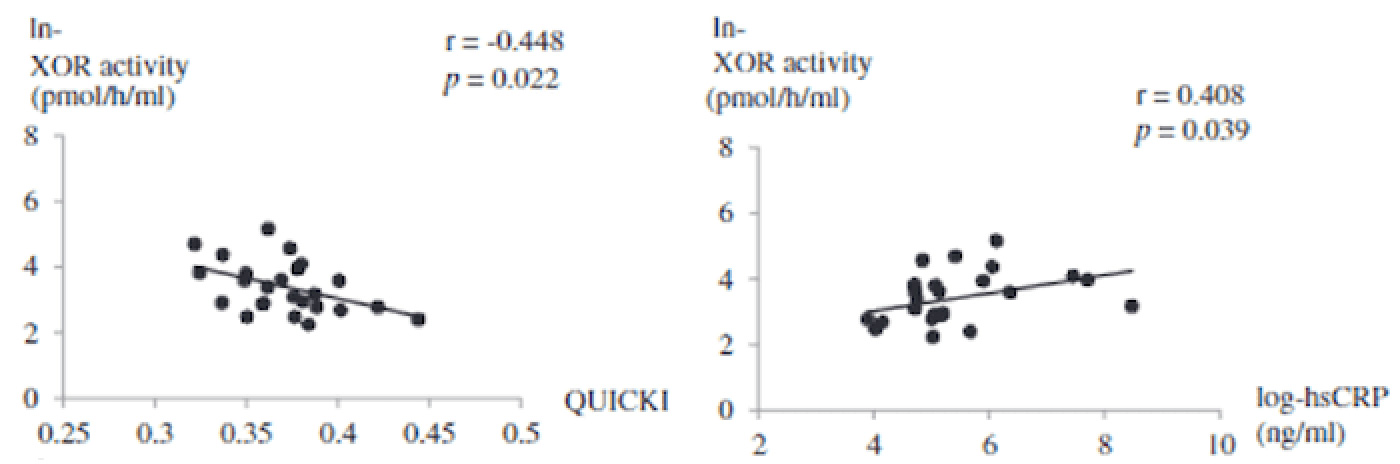
XORと動脈硬化との関連についてはこれまでに多数報告されていましたが、その基盤となる糖代謝や炎症との関連は不明でした。当科では世界に先駆けて、XOR活性がインスリン抵抗性や炎症と関連することをヒトにおいて初めて証明しました(Washio K, et al. Metabolism 2017, 70: 51-56)。
さらに、動脈硬化初期段階の病態を鋭敏に反映するとされるFMD検査を用いて、①XOR活性が1型糖尿病患者の血糖コントロールと関連すること、②尿酸値に関係なくXOR活性が血管内皮障害と関連していることも報告しました(Washio K, etal. Acta Diabetol 2020, 57: 31-9)。
また核酸代謝は内臓脂肪蓄積を基盤とするメタボリックシンドロームと関連することも指摘されています。当科ではこの点にも着目し、特に肝脂肪沈着とXOR活性との関連について検討を行っています。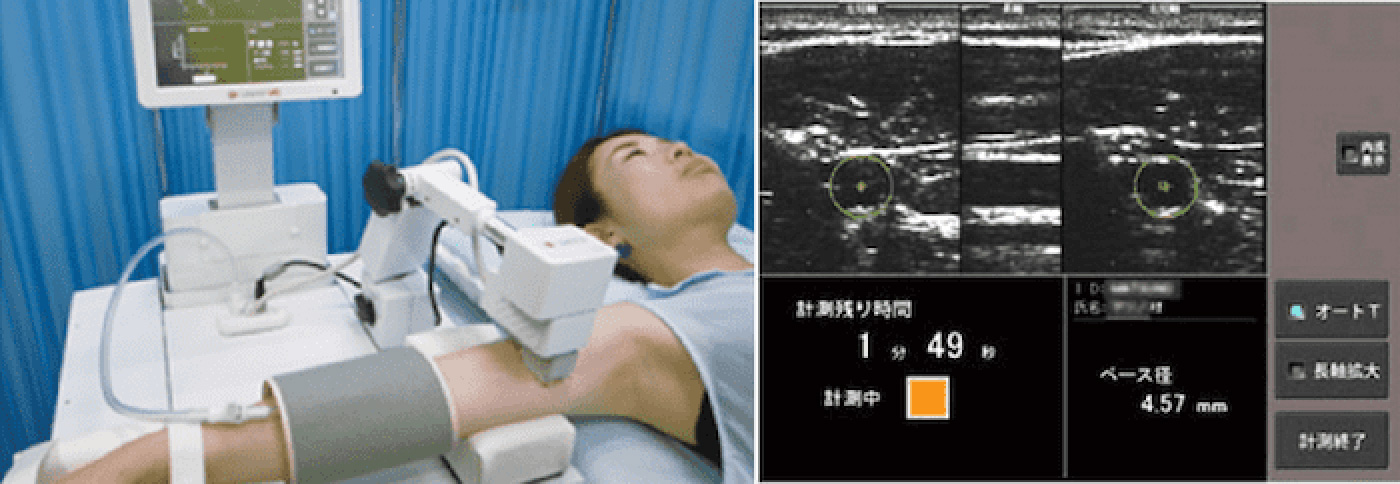
さらに、様々な条件でのXOR活性の変化と各臓器の機能変化について基礎的な検討も行っています。XOR遺伝子は、肝臓や脂肪組織における脂質代謝調節を介して肥満と関連し、加えて精神的なストレスによっても、各臓器におけるXORの発現は上昇することが知られています。
現在、当科では高脂肪食負荷モデルやストレス負荷モデルを用いて各臓器における機能及びXOR活性の変化を検討し、さらに、XOR阻害薬がこれらの影響を抑制し得るかについても検討することで、肥満や糖尿病といった様々な代謝への影響、高度なストレス社会におけるXOR活性の意義と病態への影響について研究を推進しています。
5.副腎関連疾患における睡眠・疲労度及び自律神経機能と代謝異常、動脈硬化との関連
(Hyogo Adrenal Metabolic Registry)当科は阪神地域の副腎関連疾患(主に非機能性副腎腫瘍、原発性アルドステロン症、クッシング症候群、褐色細胞腫など)の診断・治療における中核を担っています。これら副腎関連疾患では生活習慣病や動脈硬化を有する頻度が高いことが知られていますが、その詳細なメカニズムは現在も不明です。当科では、睡眠や疲労、自律神経機能といった生活関連疾患と副腎疾患との関係に注目し、HyogoAdrenal Metabolic Registryを2018年から実施しています。
これまでに、副腎からのコルチゾールの過剰分泌を有する患者では筋肉量の減少から、クレアチニンによるeGFRのみを用いた腎機能評価では過小評価されることを報告しています(Naka M, etal. Endocrine J 2020, 67, 469-476)。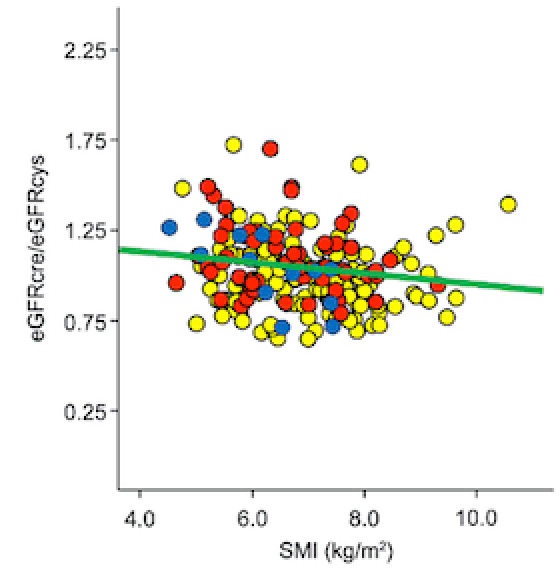
さらに当科は、日本医療研究開発機構の研究費で推進されている難治性副腎疾患の診療に直結するエビデンス創出を目的とした多施設共同研究 Japan Rare/Intractable Adrenal Diseases Study (JRAS)、疾患レジストリを活用した原発性アルドステロン症の診療の質の向上に資するエビデンス構築を目的とした多施設共同研究 Japan Primary Aldosteronism in Study II(JPAS-II)、原発性アルドステロン症の診断・治療に関する国際共同研究 GlobalPrimary Aldosteronism in Study (GPAS) に研究開発協力施設として参画しています。
また、血中ホルモン濃度と臨床症状との関連における血中蛋白の動態や測定系に対する影響を調べるため富士フィルム和光純薬株式会社との共同研究も行っています。 -
基礎研究
1.高血糖による血管炎症が引き起こされる分子メカニズムと糖尿病性血管合併症の制御
終末糖化産物受容体(receptor for advancedglycation end-products, RAGE)を中心に、メタボリックメモリーと動脈硬化分子生物学的基盤に関する研究を進めています。この研究は金沢大学との共同研究として実施しています。
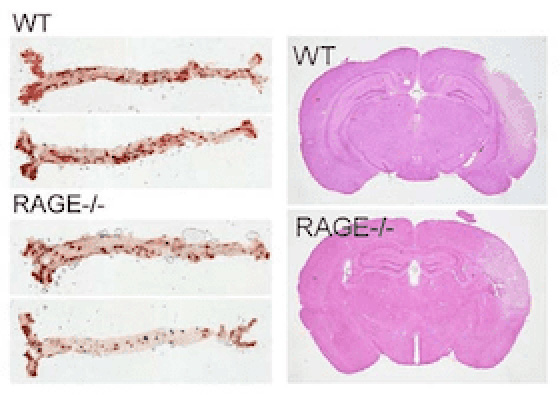
これまでの研究の中で、①アデノウイルスを用いた血管内皮へのRAGEの過剰発現により、炎症性サイトカイン(TNF-α)による炎症シグナルが亢進し炎症機転が増幅されること、②一方、血管内皮特異的にRAGEを過剰発現したトランスジェニックマウスにおいてはTNF-αなどによる炎症誘導はRAGEの切断(shedding)を誘導すること、③このTNF-αによるRAGE sheddingはJNK活性化によるマトリックスメタロプロテナーゼ(MMP)9と小胞体ストレスにかかわるATF4によるADAM10誘導により引き起こされること、を明らかにしました(Miyoshi A, et al. FASEB J. 2019, 33: 3575-3589)。
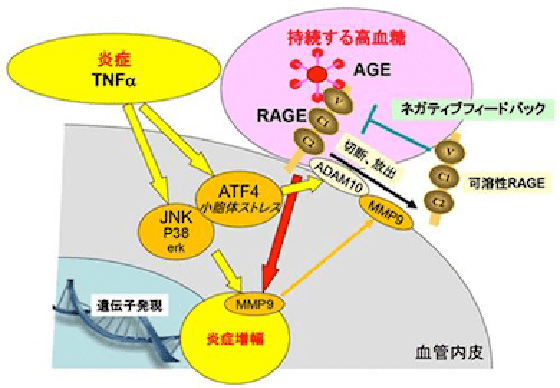
これらの結果は、持続する高血糖刺激が血管炎症を惹起し血管合併症発症に関与すること、さらに血管の炎症増幅がRAGEの切断・放出により高血糖と炎症の悪循環にブレーキをかける仕組みが存在することを示した成果で、極めて重要な知見と考えられます。
さらに高血糖と血管炎症の関連から得られた知見を発展させ、現在は脳内の慢性炎症に焦点を当て、今後の社会問題となり得る認知機能低下への影響について基礎研究を展開しています。本研究は学内の解剖学、薬理学、免疫学との共同研究として実施しています。2.睡眠の「時間」と「質」が及ぼす生体影響への違いに関する基盤研究
昨今の急速なデジタル化に加えコロナ禍での新しい日常によって我々の社会生活も大きく変化しています。睡眠に関しては「時間」だけでなく「質」の重要性が、前述した我々の臨床研究成果からも明らかになってきています。当科ではこの点に着目し、非常にユニークなマウスモデルを作製し、このモデルの病態生理学的特徴を検討してきました。
現在は主に「代謝」、「認知機能」及び「疼痛」の3点を主たるアウトカムとして、神経内分泌ホルモン、自律神経機能、神経活動などを介した調節系とその破綻について基礎的検討を行っています。中枢神経系の神経活動とその調節系の意義については、パッチクランプ法や光遺伝学的・化学遺伝学的手法を取り入れて解析しています。学内の解剖学、生理学神経生理部門及び疾患オミクス解析講座、学外では理化学研究所との共同研究として実施しています。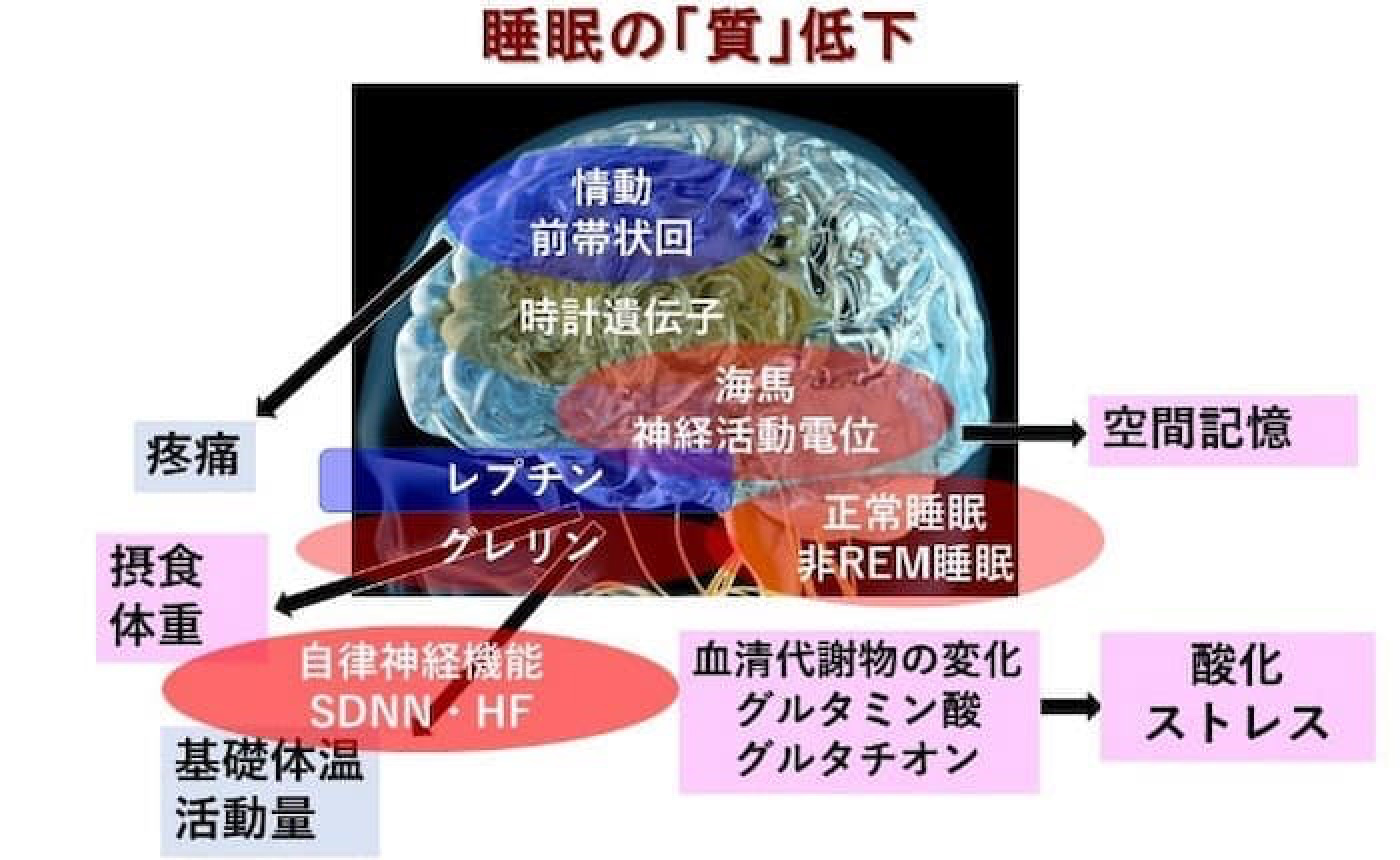
-
兵庫医科大学全学横断プロジェクト研究
Hyogo Innovative Challenge「脳内ストレス顕在化の評価を通じた疾病予防戦略と実装」を研究テーマとして、学内の複数の専門分野が協力して、基礎医学および臨床医学の両側面から、脳内ストレスの影響を解明し、関連疾患の予防策を見出すことを目指したプロジェクトです。

3年間のプロジェクトリーダーを当科の小山英則主任教授が務められました。
当科で実施中の臨床研究、基礎研究が当プロジェクトの推進に大きく貢献しました。
詳しくは専門サイトをご覧ください。

